
באדיבות וויקיפדיה
ג'ון דלטון היה מדען אנגלי משכיל שעבד בתחילת המאה ה -18, בערך בתקופה שבה בטהובן הלחין סימפוניות ונפוליאון שלט באירופה. הוא נולד למשפחה של אורגים קוויקרים בשנת 1766. בגיל 12 הוא לימד ילדים אחרים בבית הספר קווייקרי בכפר שלו. הוא המשיך ללמוד מתמטיקה, אסטרונומיה, שפות זרות ושיטות תצפית בהנחיית ג'ון גוג, פילוסוף עיוור שגר בקרבת מקום. הוא פרסם תיאוריה על זוהר הקוטב, בגיל 22. דלטון מסיק נכונה כי זוהר זה נגרם בחלקו על ידי המגנטיות של כדור הארץ. מאוחר יותר הוא פירסם תיאוריה פחות מוצלחת על הסיבות לעיוורון צבעים, אשר ממנו סבל. דלטון מעולם לא למד באוניברסיטה.
המדע לעיתים קרובות מסתכם בחיפוש אחר דפוסי מידע מתוך תצפיות. המיומנות המיוחדת של דלטון היתה היכולת לשלב בין המקורות השונים של המידע הזמין באותה עת. הוא יכול לנוע במהירות מתוך נתונים חלקיים לתובנות מבריקות ביחס ל"תמונה השלימה". בדומה לאנשים מיוחדים, היכולים לראות רק כמה חתיכות מתוך פאזל ובעזרתם לתאר את התמונה כולה. הרגעים הפתאומיים האלה של תובנה הם הרגשות הנדירים והמענגים ביותר להם זוכה המדען. דלטון צעד בעקבות הדוגמה של גלילאו, ולא רכש אמון לדעות רשויות קודמות בענייני מדע. הוא כתב "בזמן שניהלתי את חקירותי לעתים קרובות טעיתי כאשר לקחתי כמובן מאליו את התוצאות של אחרים, אני נחוש לכתוב [רק] מה אני יכול להעיד על בסיס הניסיון שלי." דלטון ערך ניסויים משלו והוא נשען על החשיבה שלו.
דלטון הגיע לתיאוריה האטומית על בסיס ניסויים שערך בגזים. באמצעות ציוד מעבדה תוצרת בית, הוא למד איך גזים מתערבבים באוויר, נמסים במים, או מתחברים זה לזה. הוא גילה כי האוויר אינו סביבה אחידה, אלא תערובת של גזים הכוללת חנקן וחמצן. גז יחיד הוא יסוד כימי. דלתון גילה כי ניתן לחבר גזים רק בפרופורציות מסוימות. חיבור גזים עשוי ליצור תרכובת כימית. לדוגמה, ניתן לחבר מימן וחמצן לשלב תוך יצירת להבה ואדי קיטור. אבל, החיבור ביניהם נעשה רק בפרופורציות מסויימות, מסת מימן אחת מול שמונה מסות של חמצן. דלטון מדד את הפרופורציות גם עבור תרכובות אחרות. הפרופורציות הספציפיות סיקרנו אותו. "אני כמעט משוכנע שהנסיבות מותנות במשקל ובמספר החלקיקים המוחלט של … גזים …" הוא כתב ב -1803.
באדיבות וויקיפדיה
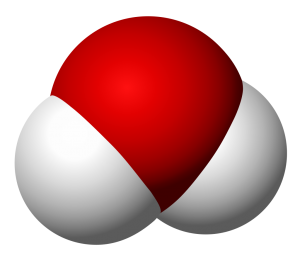
כאשר כתב על "החלקיקים המוחלטים" של כל יסוד, דלטון העניק חיים חדשים לרעיון היווני הישן בדבר קיומם של אטומים. האטום הוא אפוא החלקיק של כל יסוד שאי אפשר לחלקו באמצעים כימיים רגילים. דלטון הסיק כי משמעות הפרופורציות הקבועות, שהתרכובות נוצרו על ידי מספר קבוע של אטומים של כל יסוד, עם יסודות אחרים בעלי משקל אטומי שונה. מולקולה היא קבוצה של שני אטומים או יותר שיש ביניהם קשרים ויחד הם יוצרים תרכובת ייחודית. ניתן לאשר את מדידות של דלטון במים אם לאטומי חמצן ממשקל אטומי הגדול פי 16 מהמשקל אטומי של המימן. זאת בתנאי שלמולקולות של אדי מים (קיטור) יש שני אטומים של מימן ואטום חמצן אחד. לפיכך, דלטון היה הראשון שתאר את הרכב המים כ- H2O. כלומר, יש שני אטומי מימן ואטום חמצן אחד. בעותה עת לא היה תהליך מוכר היכול לפרק את הקשרים שבין המימן לחמצן, כך שהם נחשבו לתרכובת יסודית.
אותם רעיונות החלים על כל החומרים – מוצק, נוזל, וגז. לדוגמה, כימאים ידעו כי ניתן לחלק את מרבית החומרים לכימיקלים פשוטים יותר. שריפת עץ מייצרת פחמן דו חמצני, מים, פחמן בצורת פחם. מים ניתן לפרק בסיוע זרם חשמלי למימן וחמצן. עם זאת, לא ניתן לפרק את הפחמן לחלקיקים קטנים יותר. זהו יסוד. אנו יכולים לסכם את תובנה של דלתון לומר כי האטום הוא המקבילה המיקרוסקופית, הבלתי ניתנת לחלוקה של יסוד כימי, ומולקולה היא המקבילה המיקרוסקופית של תרכובת כימית.
דלטון פרסם את תוצאות הניסויים האלגנטיים שלו ב -1810. רעיונות אלה, הידועים כ"תורת האטום", מהווים את הבסיס לכימיה המודרנית. התיאוריה האטומית כוללת את הרעיונות המרכזיים הבאים:
כל היסודות מורכבים מאטומים.
לכל יסוד יש תכונות כימיות ייחודיות וכל יסוד מורכב מאטומים בעלי משקל ייחודי.
תרכובות נוצרות כאשר אטומים מקושרים בפרופורציות מסוימות למולקולות. לכל מולקולה יש תכונות כימיות ייחודיות.
יסודות ותרכובות מתחברים (ונפרדים) בתהליכים הנקראים תגובות כימיות.
המרכיבים המיקרוסקופיים של יסודות הם אטומים – הם יסודיים ואינם ניתנים לחלוקה לחלקיקים שונים.
לא ניתן לשנות יסוד אחד ליסוד אחר על ידי תגובות כימיות.
עבודתו של דלטון נתקלה בהתנגדות מסוימת. אחרי הכל, אף אחד מעולם לא ראה אטום בודד! הם היו כנראה קטנים מכדי להיראות במיקרוסקופ. התיאוריה האטומית היתה מכה קטלנית לאלכימיה, שהאמינה ברעיון עתיק לפיו ניתן לשנות יסוד אחד ליסוד אחר. היום אנחנו מתייחסים לאלכימיה כעיסוק בלתי-מדעי. עם זאת, במשך מאות שנים מדענים רבים ניסו להפוך מתכת כמו עופרת לזהב. הן עופרת והן זהב הן מתכות בעלות צבע עמום, כבדות וניתנות לריקוע. אין זה בלתי הגיוני לנסות להמיר אחת מהן לאחרת. ניוטון הגדול עצמו בילה מאות שעות במעבדה שלו בעריכת ניסויים באלכימיה. כיום אנחנו יודעים שתגובות כימיות יכולות לצרף או להפריד יסודות, אבל הן אינן יכולות להפוך יסוד אחד לאחר.
Author: Chris Impey

